Классификация лимфогранулематоза по формам и стадиям

Гистологические признаки определяют форму лимфомы
Ранее ЛХ именовалась болезнью Ходжкина или лимфогранулематозом. Эти названия ещё используются в практике, но по международному стандарту заболевание обозначают как ЛХ и классифицируют следующим образом:
Согласно гистологическим признакам:
- Лимфогистиоцитарная форма (15% случаев всех ЛХ). В биоптате обнаруживаются преимущественно зрелые лимфоциты, клетки БРШ представлены в малом количестве. Диагностируется обычно на начальном этапе развития, подвержены мужчины до 30 лет.
- Нодулярный (узелковый) склероз (45%). Выявляются в биоптате клетки БРШ и лакунарные клетки с большим числом ядер или одним многолопастным ядром. Характерно наличие узелков, образованных из лимфоидной ткани. Заболевание определяется чаще у женщин до 30 лет.
- Смешанно-клеточная форма (30%). В наличии клетки разной величины и видов: фибробласты, плазматические, эозинофилы, лимфоциты, клетки БРШ. Подвержены молодые мужчины, люди пожилого возраста, дети, пациенты с ВИЧ.
- Форма лимфоидного истощения (5%). Лимфоциты в биоптате отсутствуют, большое количество клеток БРШ. Болезнью страдают преимущественно люди преклонного возраста.

Количество групп пораженных лимфоузлов определяет стадию
- I — поражение 1 группы лимфоузлов либо 1 органа/ткани.
- II — поражение ≥ 2 групп лимфоузлов либо органа/ткани и лимфоузлов по одну сторону диафрагмы.
- III — поражены лимфоузлы либо орган/ткани и лимфоузлы по обе стороны диафрагмы.
- IV — смешанное, множественное поражение одного либо нескольких органов/тканей и лимфоузлов.
Стадии сопровождаются буквенными обозначениями:
- a — симптомы отсутствуют;
- b — присутствуют симптомы: повышенная температура, снижение массы тела, ночные поты;
- е — вовлечены органы/ткани, локализованные вблизи поражённых лимфоузлов;
- s — в опухолевый процесс вовлечена селезёнка;
- x — масштабное поражение.
Болезнью страдают преимущественно люди преклонного возраста.
Как лечится лимфома Ходжкина (лимфогранулематоз)?

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
В разных странах разработаны многочисленные программы лечения лимфомы Ходжкина (лимфогранулематоза). Их принципиальные элементы – лучевая терапия и полихимиотерапия с использованием относительно узкого спектра препаратов. Возможно применение только радиотерапии, только химиотерапии или комбинации обоих методов. Программы радио- и химиотерапии лимфогранулематоза постоянно совершенствуются: увеличивается их эффективность, уменьшается непосредственная и поздняя токсичность без развития резистентности. Тактику лечения лимфомы Ходжкина определяют стадия болезни и возраст пациента.
Общепринято, что лечение больных с генерализованной формой лимфомы Ходжкина (лимфогранулематоза) (стадии III и IV) начинают с полихимиотерапии. При локализованных стадиях обсуждают возможности моно- и комбинированной терапии, существуют протоколы без облученилечения с облучением инициально вовлечённых зон поражения. Данная тактика позволяет уменьшить объём и суммарную дозу облучения и химиотерапии без снижения эффективности. Принципиально важно при использовании этого метода качественно обследовать пациента, поскольку необлучение поражённых лимфатических узлов или органов почти неизбежно приводит к рецидивам, лечение которых представляет непростую задачу. При разработке химиотерапевтических протоколов необходимо соблюдать общие принципы:
- каждый из используемых препаратов должен обладать активностью против опухоли;
- комбинируют препараты с разным механизмом противоопухолевого и токсического действия в максимально допустимых дозах;
- поддерживающую терапию при лимфогранулематозе не используют, так как она не улучшает показатели выживаемости и увеличивает риск вторичных опухолей.
Предложенные в 1970-е годы режимы полихимиотерапии МОРР (мустарген, винкристин, прокарбазин и преднизолон) и ABVD (доксорубицин, блеомицин, винбластин, дакарбазин) – базовые во многих протоколах лечения лимфогранулематоза. Их используют в качестве первой линии терапии в альтернирующем режиме с различной повторяемостью, в зависимости от стадии, с облучением или без него. По данным Стенфордской Университетской детской клиники (США), 5-летняя безрецидивная выживаемость (RFS) при такой тактике составляет 95%. Тот же принцип использован Французской рабочей группой по лечению болезни Ходжкина. Вследствие высокой онкогенности мустаргена в современных протоколах его заменяют на циклофосфамид (курс СОРР), в курсы полихимиотерапии включают этопозид, ифосфамид, ломустин, цитарабин, препараты платины. Для лечения резистентных форм лимфогранулематоза всё шире используют иммунотерапию, трансплантацию гемопоэтических стволовых клеток (преимущественно аутологичную).
Результаты лечения лимфомы Ходжкина в отечественных клиниках до 1990-х годов невозможно корректно оценивать из-за отсутствия унифицированного определения стадийности и используемых методов терапии. В течение последнего десятилетия в большинстве детских специализированных клиник используют протокол лечения лимфогранулематоза, разработанный детскими онкогематологами Германии. Данный протокол показал высокую эффективность при низкой токсичности HD-DAL-90: бессобытийная выживаемость в течение 10 лет составила 81%, общая выживаемость – 94%.
 [1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]
Тактику лечения лимфомы Ходжкина определяют стадия болезни и возраст пациента.
Причины лимфомы Ходжкина
Несмотря на более чем двухсотлетнюю историю изучения этой онкологической болезни, на сегодняшний день точно ответить на вопрос, почему возникает лимфогранулематоз, невозможно.
Известно, что значимым фактором риска является наследственная предрасположенность и генные мутации клеток, из которых состоит лимфатическая система человека. Кроме того, в качестве вероятных предпосылок называют:
- наличие вируса Эпштейна-Барр либо Т-лимфотропного вируса человека;
- сбои в работе иммунной системы, частью которой является лимфатическая. Иммунодефицит может быть как врожденным, так и приобретенным. К подобным состояниям приводят аутоиммунные заболевания, ВИЧ и ряд других;
- проживание на протяжении длительного времени на радиоактивно загрязненных территориях;
- регулярный контакт с химическими веществами, являющимися потенциальными канцерогенами;
- избыточное облучение ультрафиолетом – чрезмерное пребывание на постоянной основе под прямыми солнечными лучами.
- прием некоторых медицинских препаратов.
Также определенное влияние на вероятность возникновения и развития лимфомы Ходжкина оказывает неправильный образ жизни, малая подвижность, несбалансированное питание, ожирение 2 и выше степени, злоупотребление алкоголем и никотином.
гемограмма общеклинический анализ крови, позволяющей определить отклонение от референсных значений показателей гемоглобина, лейкоцитов и СОЭ ;.
Диагностика
Раннее выявление заболевания затруднено в силу того, что клинические симптомы не имеют строго определенного характера, а часто и вовсе отсутствуют.
Диагностика лимфомы Ходжкина основана на морфологической картине пораженного лимфатического узла или органа. Назначается рад исследований:
- клинический осмотр и сбор анамнеза – особое внимание обращается на симптомы интоксикации, проводится пальпация всех периферических групп лимфатических узлов, селезенки и печени, осмотр носоглотки, миндалин;
- биопсия пораженных лимфоузлов с гистологическим и иммуногистохимическим анализом биоптата. Критерием лимфомы Ходжкина является присутствие во взятом материале специфических клеток Рида – Штернберга, незрелых клеток Ходжкина;
- лабораторные исследования – общий и биохимический анализ крови, скорость оседания эритроцитов, активность щелочной фосфатазы в сыворотке крови, почечные и печеночные пробы. В клиническом анализе крови обнаруживают повышение СОЭ, нейтрофильный лейкоцитоз, возможна умеренная эозинофилия, увеличение концентрации фибриногена, тромбоцитоз, снижение содержания альбуминов. В начальной стадии болезни в анализах крови выявляют умеренный лейкоцитоз, который по мере прогрессирования заболевания сменяется лейкопенией;
- лабораторная оценка функции щитовидной железы – при поражении шейных лимфатические узлов;
- иммунофенотипические исследования опухолевой ткани – выявляют качественные и количественные нарушения Т-клеточного звена иммунитета.
- рентгенологические исследования грудной клетки, скелета, желудочно-кишечного тракта – имеют ведущее значение в определении характера и выявлении локализации поражений;
- УЗИ брюшной полости – с той же целью, что и рентгенография;
- компьютерная томография, магниторезонансная томография шеи, органов грудной клетки, живота и таза – позволяет выявить наличие опухолевых образований в разных частях тела;
- трепанобиопсия – проводится при подозрении на поражение костного мозга подвздошных костей;
- остеосцинтиграфия – при повышенном уровне щелочной фосфатазы в сыворотке крови;
- диагностическая лапаротомия – применяется для взятия биоптатов мезентериальных и парааортальных лимфатических узлов.
Назначается рад исследований.
Личный опытКак я боролась с лимфомой Ходжкина: От первых симптомов до ремиссии
«Страх — это нормально, но не нужно отдавать ему свою жизнь»
- 30 ноября 2016
- 129460
- 18

Текст: Татьяна Горюнова
В детстве я любила лежать с мамой в обнимку, уткнувшись в её пепельные волосы. Я гладила её по голове и разглядывала шрам на шее, гадая, откуда же он мог взяться, придумывала невероятные сказочные истории, а мама всегда соглашалась и восхищалась моей фантазией. Когда я стала старше, в голове начали всплывать воспоминания: мамино истощённое тело, нежелание встать и оценить мой шедевр из LEGO, её ночные лихорадки, резкая смена причёски. Спустя годы, как это свойственно подросткам, я задала прямой вопрос и получила исчерпывающий ответ: «Лимфома». Я была шокирована, но в то же время наконец перестала мучиться догадками. С тех пор изредка всплывавшие новости о больных онкологией меня сильно волновали и безумно трогали, так как болезнь прошла совсем рядом. Я очень гордилась мамой, но по молчаливому согласию было решено не обсуждать это в семье и за её пределами.

Весной 2015 года мне начали сниться кошмары про мёртвых животных, личинки, больничные палаты и операционные, выпадающие зубы. Сначала я не обращала внимания, но позже, когда сны стали регулярными, у меня возникла навязчивая мысль лечь в больницу на полное обследование. С близкими я делилась мыслями о том, что мозг может таким образом посылать сигнал о болезни, но меня убедили, что не нужно быть мнительной и придумывать глупости. И я успокоилась. Летом я исполнила давнюю мечту пересечь Америку на машине от океана до океана. Друзья были в восторге, а моё впечатление смазывали чувство дикой усталости, постоянная одышка и боли в грудной клетке. Я списывала всё на лень, жару и набранные килограммы.
В октябре я вернулась в солнечную Москву, и, казалось бы, должна быть полна впечатлений и сил после отдыха. Но я просто загибалась. На работе было невыносимо, усталость была такой, что после рабочего дня я мечтала лишь скорее оказаться в кровати. В метро находиться было пыткой: кружилась голова, постоянно темнело в глазах, я падала в обмороки и заработала пару шрамов на висках. Меня мутило от посторонних запахов, будь то духи, цветы или еда. Я одёргивала себя и ругала за то, что никак не могу войти в привычный жизненный ритм.
Один из тех вечеров я провела с другом, которого давно не видела: ужин, вино, шутки, воспоминания и бесконечные петли разговора, заставившие меня остаться на ночь. Наутро, собирая свои длинные волосы перед умыванием, я задела шею и заметила опухоль размером с апельсин. В ту же самую секунду выдвинула точное предположение о том, что это, но осталась на удивление спокойна, а затем одёрнула себя словами: «Нет, такое может случиться с кем угодно, но только не со мной». За завтраком друг обратил внимание на опухоль и высказал предположение, что это может быть аллергия; я согласилась, но в голове начали мелькать воспоминания, толкающие к слову «рак».
По дороге на работу я наконец осознала серьёзность происходящего и поняла, что мне надо немедленно ехать к врачу. Я вспомнила мамин шрам — ровно на месте моей опухоли. Сквозь рой беспорядочных мыслей я слышала, как друг пытался меня подбодрить и нелепо шутил, но от этого мне становилось всё страшнее, и я почувствовала, как к горлу подступает ком, а на глаза наворачиваются слёзы.
Пару часов спустя я безо всяких эмоций сидела в холодном коридоре на скамейке в районной поликлинике. После некоторого замешательства терапевт сделал заключение: «У вас, скорее всего, аллергия — не о чем беспокоиться, попейте антигистаминный препарат». Я рассказала о маминой болезни, высказывала предположение о том, что стоит сделать УЗИ, но в ответ врач произнёс фразу, которая ввела меня в ступор: «У нас все направления по квотам, ты выглядишь здоровой — вон какие румяные щёки — нет у меня оснований тебе его давать, ступай». Позже я ещё много раз сталкивалась с равнодушием, некомпетентностью и халатностью врачей в государственных поликлиниках.
Зима. Всё закрутилось после того, как я, не слушая никого, всё-таки сделала компьютерную томографию. На снимке отчетливо были видны конгломераты огромных лимфоузлов в шее и грудной клетке, увеличенные сердце и селезёнка. Радиолог отправил меня к онкологу, а онколог — к гематологу. Последний похвалил меня за настойчивость и бдительность и подтвердил мои догадки, настоятельно посоветовав вырезать часть опухоли для исследования (точный диагноз ставят после биопсии и гистологического исследования). После операции я услышала медицинский код «С 81.1», обозначающий мою болезнь. Мне пришлось преодолеть многое, чтобы наконец узнать правильный диагноз и приступить к долгожданному лечению.
Лимфома Ходжкина (её ещё называют лимфогранулематозом) — это онкологическое заболевание. Интересно, что в медицинском сообществе её не называют раком, так как раковая опухоль образуется из эпителиальной ткани, а клетки крови и лимфоидная ткань, из которых образуется лимфомная опухоль, к ним не относятся. Но по своему развитию, течению и воздействию на организм лимфомы бывают агрессивными, так же как и рак, и способны поражать другие органы и системы, помимо иммунной. Поэтому, если не углубляться в медицинские термины, говорят, что это «рак лимфатической системы». Так проще понять, о чем идёт речь и насколько серьёзно заболевание. Точной причины возникновения лимфомы Ходжкина пока не выявлено, иногда болезнь ассоциируют с вирусом Эпштейна — Барр. Лимфогранулематоз считается болезнью молодых, так как первый всплеск заболеваемости приходится на 15–30 лет. В настоящее время прогнозы выживаемости при обнаружении болезни на ранних стадиях довольно позитивные. Может быть, именно поэтому я с самого начала была уверена, что у меня всё получится, а может быть, помог пример моей мамы.
От этого я не могла есть каждый глоток воды или мельчайший кусок пищи ощущался как кактус.
Классификации
Согласно общепринятой международной классификации, болезнь Ходжкина имеет следующие морфологические варианты:
- Лимфоидное преобладание, обозначенное как С81.0 (временная форма)
- Нодулярный склероз с кодом С81.1. Наиболее распространенная форма – 50% всех случаев, характеризуется появлением плотных соединительнотканных тяжей, разделяющих лимфатические органы на «узлы». При патоморфологическом исследовании обязательными элементами этой формы являются клетки Березовского-Штернберга и лакунарные клетки. Эта форма лимфогранулематоза у женщин встречается чаще.
- Смешанно-клеточный тип по мкб С81.2. Соответствует второй и третей стадии болезни и составляет примерно 30% от всех случаев. При исследовании биологического материала определяется множество форм лимфоцитов, плазмоцитов, фибробластов и т.д. Разный клеточный пул способствует ускоренной генерализации патологического процесса.
- Лимфоидное истощение С81.3
- Другие формы Ходжскинских лимфом С81.7
- Болезнь Ходжкина неуточненная закодированная как С81.9
Каждый вариант при лимфогранулематозе имеет стадии течения, которые отражают распространенность патологического процесса по человеческому телу.

- Первая стадия Ходжскинской лимфомы характеризуется локальным вовлечением в патологический процесс лимфатических узлов из одной анатомической группы и поражением 1 органа за пределами лимфоузлов.
- При лимфогранулематозе 2 стадии поражаются лимфоузлы из 2 и больше групп по одну сторону от диафрагмы, а также органа и лимфоузлов с подобной локализацией.
- Лимфома Ходжкина 3 стадия характеризуется поражением лимфоидной ткани по обе стороны от диафрагмы, как с поражением селезенки, так и без вовлечения внутренних органов.
- Лимфома Ходжкина 4 стадия диффузно поражает органы брюшной, грудной полостей, костный мозг и др. и множественное поражение лимфоузлов из разных анатомических областей или без вовлечения в онкологический процесс последних.
Лимфома Ходжкина 3 стадия характеризуется поражением лимфоидной ткани по обе стороны от диафрагмы, как с поражением селезенки, так и без вовлечения внутренних органов.
Распространенность заболевания
Лимфома Ходжкина возникает с частотой 1-3 случая на 100 000 человек в год. В общей сложности около 2200 человек в России заболели лимфогранулематозом в 2015 году. Мужчины заболевают в 1,5 раза чаще, чем женщины.
Болезнь может возникать в любом возрасте. Лимфома Ходжкина, хотя и редкая по сравнению с большинством других видов рака, является одним из наиболее распространенных видов рака у молодых людей.
После употребления алкоголя увеличенные лимфоузлы могут вызвать боль в спине; состояние возникает очень редко, но относительно характерно для лимфомы Ходжкина.
Лимфогранулематоз у детей
Это редкая болезнь у детей от шести до шестнадцати лет. Заболевание начинается часто с того, что на шее у ребёнка вскакивает безболезненная шишка — увеличенный лимфоузел. Также возможно, но реже, появление такого узла в области средостения (грудины) и ещё реже в брюшной или паховой области. Другие симптомы лимфомы могут поначалу отсутствовать.
- температура;
- ночная повышенная потливость;
- плохой аппетит и сон;
- частые болезни ребёнка.

Из клинических признаков может быть увеличенная селезенка, однако прощупать её удаётся не всегда. Гепатомегалия считается неблагоприятным признаком.
Лимфогранулематоз у детей требует как можно более ранней диагностики и лечения: один или два узла до появления системных симптомов необходимо удалить, после чего провести курс облучения.
Поражение многих лимфоузлов и органов требуют другой схемы лечения с применением химиотерапии. Один из вариантов лечения детей — аутотрансплантация костного мозга.
Лимфогранулематоз у детей требует как можно более ранней диагностики и лечения один или два узла до появления системных симптомов необходимо удалить, после чего провести курс облучения.
Общие сведения
Лимфогранулематоз (ЛГМ) – лимфопролиферативное заболевание, протекающее с образованием специфических полиморфно-клеточных гранулем в пораженных органах (лимфоузлах, селезенке и др.). По имени автора, впервые описавшего признаки заболевания и предложившего выделить его в самостоятельную форму, лимфогранулематоз также называют болезнью Ходжкина, или ходжкинской лимфомой. Средний показатель заболеваемости лимфогранулематозом составляет 2,2 случая на 100 тыс. населения. Среди заболевших преобладают молодые люди в возрасте 20-30 лет; второй пик заболеваемости приходится на возраст старше 60 лет. У мужчин болезнь Ходжкина развивается в 1,5-2 раза чаще, чем у женщин. В структуре гемобластозов лимфогранулематозу отводится втрое место по частоте возникновения после лейкемии.
Причины лимфогранулематоза.
I стадия
На начальной стадии поражена одна группа узлов, обычно в верхней половине тела, либо один внутренний орган. Симптомы клинической картины у больного зачастую не обнаруживаются, а факт увеличенных узлов больной может неожиданно обнаружить для себя при проведении планового медосмотра.
Причины развития.
Современное лечение лимфомы Ходжкина (лимфогранулематоза)
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Российский онкологический научный центр им. Н.Н. Блохина РАМН
К концу ХХ века 10–летняя безрецидивная выживаемость больных лимфомой Ходжкина, по данным крупных исследовательских центров, при ранних стадиях достигла 90%: EORTC (Европейская организация по исследованию и лечению рака), 1993 г. – 92%, Stanford, 1997 г. – 93%, Harvard, 1999 г. – 96%, РОНЦ, 1988 г. – 89%. При распространенных стадиях 5–летняя выживаемость при этом заболевании, по данным NCI (Национальный раковый институт, США), 1999 г. достигает 60% [1,5]. В течение двух последних десятилетий прошлого века проводились многочисленные клинические исследования – велся целенаправленный поиск наилучшей комбинации химиотерапии и оптимального сочетания лучевой и химиотерапии при лечении больных лимфомой Ходжкина (название употребляется в соответствии с классификацией лимфом, принятой ВОЗ в 2001 г.). Анализ этих исследований позволил предложить новую комбинацию факторов риска и иное разделение больных по прогностическим группам при выборе программы лечения. Появились и новая стратегия лечения, и новые терапевтические программы.
С конца 70–х годов в зарубежной литературе вместо терминов «локализованные» и «генерализованные» стадии стали использоваться термины «early» – ранние и «advanced» – распространенные (продвинутые) стадии в значении местно–распространенный/диссеминированный процесс (аналогично терминологии при солидных опухолях). Обоснованием для этих терминов стал анализ результатов радикальной лучевой терапии лимфомы Ходжкина, при котором было показано, что эффективность лечения зависит от общей массы опухоли: при поражении только одной анатомической зоны лимфатических коллекторов 10–летняя безрецидивная выживаемость достигала 80%, в то время как при поражении 4 и более зон – лишь 23% [5]. Кроме того, 10–летняя безрецидивная выживаемость больных с I–II стадиями и массивным поражением средостения оказалась такой же низкой (56%), как у больных с распространенными стадиями (62%) [5]. С онкологической точки зрения этот факт легко объясняется тем, что эффективность лечения всех опухолей, и лимфомы Ходжкина в том числе, зависит от общей массы опухоли. При IIIА стадии с небольшими числом, малыми размерами лимфатических узлов и двумя зонами поражения общая масса опухоли меньше, чем при I или II стадиях с массивным поражением средостения.
В конце 70–х годов на смену радикальной лучевой терапии при I–III А стадиях лимфомы Ходжкина приходит комбинированное химио–лучевое лечение. К этому времени по результатам радикальной лучевой терапии определены прогностические факторы для I–II стадий лимфомы Ходжкина [6,9]. Набор прогностических факторов несколько варьировал у различных исследовательских групп, но в целом к неблагоприятным прогностическим факторам для I и II стадий были отнесены следующие факторы: возраст старше 40 (или 50) лет, поражение 3 и более лимфатических областей (или 4 и более), СОЭ выше 30 мм/час при наличии симптомов интоксикации и выше 50 мм/час при их отсутствии, гистологические варианты смешанноклеточный и лимфоидное истощение, а также массивное (медиастинально–торокальный индекс (МТИ) более 0,33) поражение медиастинальных лимфатических узлов. Эти прогностические факторы разделяли только больных с I и II стадиями лимфомы Ходжкина на две группы, нуждающиеся в различном объеме лечения.
В связи с тем, что понятие «поражение 3 и более лимфатических областей» неоднозначно трактовалось разными исследователями, на V международном симпозиуме по лимфогранулематозу в сентябре 2001 года было обращено особое внимание на различие терминов «area» – область и «region» – зона. Было уточнено, что термином «зона» (region) обозначаются анатомические зоны, по которым устанавливается стадия заболевания в соответствии с классификацией, принятой в Ann–Arbor. Термин «область» (area) – более широкое понятие, область может включать в себя одну или более зон. Так, в одну область были включены шейные, над– и подключичные лимфатические узлы с одной стороны. Также в одну область объединены медиастинальные лимфатические узлы и лимфатические узлы корней легких; одной областью считаются лимфатические узлы «верхнего этажа» брюшной полости (ворота печени, ворота селезенки и корень брыжейки) и одной областью – лимфатические узлы «нижнего этажа» брюшной полости (парааортальные и мезентериальные).
Во второй половине 90–х годов EORTC и Германской группой по изучению лимфомы Ходжкина (GHDG) был проведен многофакторный анализ прогностических факторов. В исследование было включено более 14000 больных [5]. Этот анализ показал, что для всех больных лимфомой Ходжкина при использовании химиотерапии и комбинированного лечения, кроме стадии заболевания и симптомов интоксикации, прогностически значимыми являются только следующие факторы:
1. Массивное поражение средостения (МТИ >0,33).
2. Массивное поражение селезенки (наличие 5 и более очагов или увеличение органа с его диффузной инфильтрацией).
3. Экстранодальное поражение в пределах стадии, обозначаемой символом «Е».
4. Поражение трех или более областей лимфоузлов.
5. Увеличение СОЭ>30 мм/час при стадии Б и >50 мм/час при стадии А [2,3,5].
Эти факторы в совокупности со стадией заболевания и симптомами интоксикации позволили исследователям из GHDG разделить больных лимфомой Ходжкина на прогностические группы. В соответствии с объемом опухолевой массы были выделены три прогностические группы – с благоприятным, промежуточным и неблагоприятным прогнозом (табл. 1), и тем самым выбор программы лечения был поставлен в прямую зависимость от объема опухолевой массы.

Адекватные дозы лучевой терапии на каждое лучевое поле для лимфомы Ходжкина были разработаны H. Kaplan в 60–х годах. Именно он показал, что при дозе облучения в 30 Гр риск рецидива в облученном поле составляет всего 11%, а в интервале доз от 35 до 40 Гр снижается лишь до 4,4%, но 100–процентная эффективность все равно не достигается при дальнейшем повышении дозы облучения. Еще трижды, в середине 70–х годов Fletcher G.H. и Shukovsky L.G., в начале 90–х годов Brincker H. и Bentzen S.M. и в конце 90–х годов M.Loeffler с соавторами проводили анализ эффективности различных доз лучевой терапии для больных с лимфомой Ходжкина [2,3,5,6]. Все три исследования на большом клиническом материале подтвердили выводы, сделанные H. Kaplan, о достижении максимальной тумороцидной дозы в интервале между 30 и 40 Гр и нецелесообразности превышения дозы локального облучения выше 40 Гр, в том числе и на большие опухолевые массы. Brincker H. и Bentzen S.M. при анализе всех опубликованных исследований с 1960 по 1990 гг. показали, что при проведении только радикальной лучевой терапии 95% контроль за лимфомой Ходжкина достигается для лимфатических узлов размером менее 6,0 см при дозе 26,5 Гр, а для лимфатических узлов более 6,0 см при дозе 32,5 Гр [6]. Эти данные были подтверждены клиническим исследованием M.Loeffler с соавторами (1997 г.), которое показало, что при использовании 20 Гр, 30 Гр и 40 Гр на зоны исходно пораженных лимфатических узлов (на большие массивы доза облучения всегда достигала 40 Гр) в рамках комбинированной химио–лучевой терапии не выявлено различия в результатах лечения: 4–летняя выживаемость, свободная от неудач лечения, составила 86%, 80% и 90% соответственно, а общая выживаемость – 93%, 94% и 88% (р=0,5) [5].
До настоящего времени при лечении первичных больных лимфомой Ходжкина использовались две основные схемы полихимиотерапии – схема МОРР (и ее аналоги) и схема ABVD. Длительный, 30–летний спор о преимуществе одной из схем был решен в последнее десятилетие в пользу программы ABVD. В конце 80–х – начале 90–х годов три крупные исследовательские группы опубликовали результаты больших рандомизированных исследований. Эти исследования показали статистически значимое преимущество комбинированных программ, в которых использовалась полихимиотерапия по схеме ABVD, по сравнению с программами со схемой МОРР. В исследовании EORTC (1997 г.) при одинаковой 10–летней общей выживаемости (больные с I–II стадиями лимфомы Ходжкина и неблагоприятным прогнозом, 6 циклов полихимиотерапии и лучевая терапия) риск неудачи лечения к 10 годам составил 24% для больных, получавших химиотерапию МОРР, и 12% для больных, получавших химиотерапию ABVD (p 2 , блеомицин 10 мг/м 2 , винбластин 6 мг/м 2 , дакарбазин 375 мг/м 2 , все препараты вводятся в 1 и 15–й дни с интервалом в 2 недели) была признана приоритетной для первичных больных с лимфомой Ходжкина.
В последние десятилетия комбинированное химио–лучевое лечение прочно заняло лидирующее положение в лечении всех первичных больных лимфомой Ходжкина.
Для первичных больных лимфомой Ходжкина основной идеологией терапии стало положение: «Объем лечения соответствует объему поражения». Разделение больных на три прогностические группы облегчает выбор адекватной программы лечения.
Лечение больных с благоприятным прогнозом
Эта группа больных малочисленна и требует небольшого объема лечения. Во всех исследованиях длительная (10–летняя и более) выживаемость в этой группе достигает 96–100%. За последние два десятилетия в этой группе больных несколькими крупными рандомизированными исследованиями было доказано преимущество комбинированной терапии. В исследовании EORTC 6–летняя выживаемость, свободная от неудач лечения, составила в группе комбинированного лечения 90%, в то время как в группе, получавшей радикальную лучевую терапию, лишь 81% – p 2 1–й и 8–й дни, адрибластин 35 мг/м 2 1–й и 15–й дни, преднизолон 50 мг внутрь с 1–го по 28 день ежедневно, этопозид 100 мг/м 2 в/в с 15–го по 19 день ежедневно, блеомицин 10 мг/м 2 1–й и 8–й дни). После двухнедельного интервала следует лучевая терапия на зоны исходного поражения. Вся программа выполняется за 10 недель [5]. В 1978–88 гг. в РОНЦ им. Н.Н. Блохина РАМН также проводилось рандомизированное исследование по лечению этой группы больных (85 человек). Сравнивалась комбинированная терапия (4 цикла CVPP + облучение зон исходного поражения) и радикальная лучевая терапия. Шестилетняя выживаемость, свободная от неудач лечения, составила 88% и 63% соответственно – p
Лечение больных промежуточной прогностической группы
Эта группа больных лимфомой Ходжкина наиболее многочисленна, и принципиальное преимущество комбинированной терапии для этой группы больных было доказано еще к началу 90–х годов. В рандомизированном исследовании EORTC (1977–1982 гг.) 15–летняя общая выживаемость оказалась одинаковой – 69%, но риск рецидива на этот срок в группе больных, получавших радикальную лучевую терапию, составил 35% по сравнению с 16% в группе комбинированного лечения – p
Лечение больных неблагоприятной прогностической группы
Для лечения этой группы больных всегда использовалась полихимиотерапия. Непосредственная эффективность лечения достигала 60–80% полных ремиссий, но 5–летняя выживаемость редко превышала 60%, а выживаемость, свободная от неудач лечения, достигла лишь 40% [2,3,5]. В начале 80–х годов две группы исследователей (из Ванкувера и из Милана) предложили объединить в одной программе обе схемы полихимиотерапии первой линии (MOPP и ABVD) для повышения эффективности терапии. В 80–х – начале 90–х годов 9 крупных исследовательских групп провели многоцентровые рандомизированные исследования, пытаясь доказать преимущество 7–8–компонентной полихимиотерапии перед 4–компонентной. Только в 3 из 9 исследований было показано незначительное преимущество многокомпонентной химиотерапии перед 4–компонентной по безрецидивной выживаемости, однако остальные 6 исследований не выявили никаких различий [4,5].
В начале 90–х годов две группы исследователей – из Стэнфорда и из Германии (GHSG) – независимо друг от друга предложили новую концепцию для лечения этих больных. Проанализировав предшествовавшие программы лечения в большой группе больных (более 700 человек в группе GHSG), эти исследователи предложили иные принципы интенсификации лечения. Кроме объединения в одной схеме основных препаратов первой линии и эскалации доз, был сокращен интервал между циклами химиотерапии, чем достигалась более высокая еженедельная дозная нагрузка в течение всей программы лечения. Широкое внедрение в лечебную практику гранулоцитарных и макрофагальных колониестимулирующих факторов (граноцит, нейпоген, лейкомакс) позволило проводить всю программу лечения в оптимальном режиме без удлинения интервалов.
Стэнфордская группа предложила программу Stanford V, а GHSG – схемы ВЕАСОРР–базовый и ВЕАСОРР–эскалированный с добавлением лучевой терапии в дозе 30–36 Гр на зоны исходно больших массивов и/или остаточные опухолевые массы. Программа Stanford V состоит из 12–недельной беспрерывной полихимиотерапии и последующей лучевой терапии у больных, не достигших полной ремиссии. Лечение получили 126 больных и при 4,5–летней медиане наблюдения прогнозируемая 8–летняя общая выживаемость составила 96%, а выживаемость, свободная от неудач лечения – 89% [5]. GHSG предложила программу, состоящую из 8 циклов полихимиотерапии ВЕАСОРР базового или эскалированного уровня с последующим облучением. Эта исследовательская группа представила наиболее убедительные доказательства преимущества нового принципа лечения в рандомизированном многоцентровом исследовании. Было проведено сравнение 8 циклов ВЕАСОРР базового (циклофосфамид 650 мг/м 2 в 1–й день, адрибластин 25 мг/м 2 в 1–й день, вепезид 100 мг/м 2 1–3–й дни, прокарбазин 100 мг/м 2 1–7 дни, преднизолон 40 мг/м 2 1–8 дни, блеомицин 10 мг/м 2 в 8–й день и винкристин 1,4 мг/м 2 в 8–й день, курс возобновляется на 21–й день) и эскалированного (по дозам адрибластина, вепезида и циклофосфамида) уровней, со стандартной полихимиотерапией СОРР/ABVD (4 двойных цикла). Облучение зон исходно больших массивов и/или остаточных опухолевых масс проводилось во всех трех сравниваемых программах. Всего в исследование было включено 689 больных. Частота полных ремиссий составила 83%, 88% и 95% в группах больных, получавших полихимиотерапию СОРР/ABVD, ВЕАСОРР–базовый и ВЕАСОРР–эскалированный. Статистически значимо больше было больных с прогрессированием заболевания в группе, получавшей СОРР/ABVD – 13% по сравнению с 9% и 2% соответственно в группах, получавших ВЕАСОРР–базовый и ВЕАСОРР–эскалированный, что и обеспечило лучшую 2–летнюю выживаемость, свободную от неудач лечения в группах, получавших ВЕАСОРР: 72%, 81%, 89% соответственно, р Заключение
Таким образом, прошедшее столетие показало возможность излечения большинства больных лимфомой Ходжкина, а на рубеже столетий были сформулированы новые концепции лечения этих больных. Ушли в прошлое радикальная лучевая терапия и широкопольное облучение. Лучевая терапия стала применяться для всех больных только в сочетании с химиотерапией, исключительно на зоны поражения и в дозах не выше 30–40 Гр. Четко определилась тенденция к дальнейшему снижению суммарных очаговых доз облучения.
Основным лечебным принципом стало соответствие объема терапии объему опухолевой массы. Разделение больных на прогностические группы в соответствии с объемом опухолевой массы позволило более адекватно выбирать программу лечения. Так, для благоприятной прогностической группы с минимальным объемом поражения показан минимальный объем лечения – 2–4 цикла химиотерапии + облучение только исходно пораженных лимфатических коллекторов; для промежуточной прогностической группы – 4–6 циклов полихимиотерапии + облучение только исходно пораженных зон; для неблагоприятной прогностической группы с большим объемом опухоли максимальный объем лечения – 8 циклов полихимиотерапии + облучение зон исходно больших массивов и/или зон с остаточными лимфатическими узлами.
1. Клиническая онкогематология.// Ред. Волкова М.А. // Москва, Медицина, 2001.
2. Bailliere’s Clinical Haematology. International Practice and Research. Hodgkin’s Disease. // Guest editor V. Diehl. – 1996.
3. Cancer. Principles & Practice of Oncology. 4th Edition. // Ed. by V.T.DeVita, S. Hellman, S.A. Rosenberg // Philadelphia. – 1993. – V 2. – Р. 1819–1858.
4. Diehl V., Franklin J., Hansenclever D. et al. // Ann. of Oncol. – 1998. – V 9. (Suppl 5). – P. 68 – 71.
5. Hodgkin’s disease. // Ed. by Mauch P.V., Armitage J.O., Diehl V. et al // Philadelphia. – 1999.
6. Brincker H., Bentzen S.M.//Radiotherapy & Oncology, 30 (1994), 227–230.
7. Ruffer J–U., Sieber M., Pfistner B., et al.// Leukemia & Lymphoma –2001. – V 42 (Suppl. 2). – Abstr. P–095.– P.54
8. Zittoun R., Audebert A., Hoerni B. Et al.// J. Clin/ Oncol. – 1985. – V 3. – P. 203–214.
В начале 80 х годов две группы исследователей из Ванкувера и из Милана предложили объединить в одной программе обе схемы полихимиотерапии первой линии MOPP и ABVD для повышения эффективности терапии.
Лимфома Ходжкина (Лимфогранулематоз) — причины, симптомы и лечение. Сколько живут с лимфомой Ходжкина?
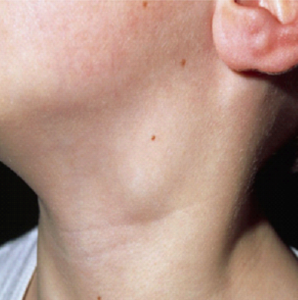 Лимфома Ходжкина (Hodgkin lymphoma) или лимфогранулематоз (ЛКБ) представляет собой одну из разновидностей злокачественной неоплазии, оказывающей разрушительное воздействие на работу системы лимфатических узлов и их сосудов. В результате повреждения лимфоидной ткани, клетки начинают бесконтрольно делиться и деструктивно воздействовать на функции нервных волокон и лимфоузлов. Индикатором наличия именно этого заболевания становится обнаружение, при биопсическом анализе опухоли, огромных по своим размерам клеток под названием Рид-Березовского-Штернберга или Ридштернберг (опухолевые клетки, рассеянные по реактивным клеткам организма и не имеющие способности вырабатывать иммунитет).
Лимфома Ходжкина (Hodgkin lymphoma) или лимфогранулематоз (ЛКБ) представляет собой одну из разновидностей злокачественной неоплазии, оказывающей разрушительное воздействие на работу системы лимфатических узлов и их сосудов. В результате повреждения лимфоидной ткани, клетки начинают бесконтрольно делиться и деструктивно воздействовать на функции нервных волокон и лимфоузлов. Индикатором наличия именно этого заболевания становится обнаружение, при биопсическом анализе опухоли, огромных по своим размерам клеток под названием Рид-Березовского-Штернберга или Ридштернберг (опухолевые клетки, рассеянные по реактивным клеткам организма и не имеющие способности вырабатывать иммунитет).
Код данного заболевания по МКБ — 10 C81.
Обратите внимание: Риск столкнуться с заболеванием лимфогранулематоза достаточно высок для людей в возрастном диапазоне от 14 до 40 лет, при этом, лимфоме Ходжкина по статистике больше подвержены мужчины, чем женщины.
- Происхождение Лимфомы Ходжкина и ее разновидности
- Почему возникает заболевание?
- Признаки
- Лимфома Ходжкина у детей
- Лимфогранулематоз и беременность
- Как диагностировать заболевание?
- Способы лечения лимфогранулематоза
- Питание при лимфоме Ходжкина
- Степень эффективности лечения
- Осложнения после лечения
- Видео: Лимфома Ходжкина
Почему возникает заболевание.
Систематические проявления заболевания Ходжкина
Системные проявления заболевания Ходжкина подразумевают периодическое появление у пациента следующих симптомов:
- повышенная температура тела до показателей 38-400 с постоянным ощущением озноба и мышечными болями. Нормализация температуры тела происходит быстро, но сопровождается обильным потоотделением. Данный симптом у пациентов с лимфогранулематозом можно заметить 1 раз в несколько дней, и с переходом заболевания в более глубокую стадию такой интервал становится все меньше;
- снижение веса (до 10% от изначальной массы тела в течение 6 месяцев);
- плохая переносимость вирусных инфекций. Больные с лимфомой Ходжкина часто страдают ветряной оспой, грибковыми (например, кандидоз) и бактериальными инфекциями;
- слабость и быстрая утомляемость. Нарушение концентрации внимания, плохая переносимость физических нагрузок, сонливость вызываются ростом канцерогенных клеток и попытками организма противостоять патологии. Особенно сильно ощущается на 3-4 стадии заболевания.
Данный метод исследования может быть дополнительно назначен врачом для оценки кроветворной функции мозга и возможного обнаружения клеток Березовского-Штернберга.
Особенности заболевания
Достоверно причины лимфогранулематоза до сих пор не были определены.
Помимо лимфоузлов лимфома Ходжкина способна поражать и ткань легких. Когда заболевание обнаруживают, то распознают и растущие в бронхах очаги или инфильтраты. Не всегда подобное сопровождается какими-либо симптомами, поэтому откладывается и лечение, что в будущем может негативно сказаться на прогнозе. В 30% случаев поражению подвергается и селезенка, причем даже при 1 и 2 стадии.
Часто при исследованиях выявляют в плевральных полостях жидкость. В ней самой обнаруживаются специфические клетки лимфомы. Само поражение чаще всего проявляется при лимфогранулематозе в области средостения. В таких случаях существует опасность прорастания опухоли в перикард, трахею, миокард или пищевод.
Поражению в 20% случаев подвергается и костная система. По большей части вероятно проникновение раковых клеток в позвонки, грудную область, таз, а реже всего патологии подвергаются трубчатые кости. Поражение костной ткани выявляется на последней стадии и сопровождаются болями. Бессимптомно протекать может распространение лимфогранулематоза на костный мозг.

Поздно диагностируют поражение печени, поскольку длительное время из-за компенсаторной функции органа не появляются какие-либо признаки.
Вторично страдает ЖКТ, что связано со сдавлением или постепенным прорастанием опухоли. Иногда метастазы определяются в самом желудке или же тонкой кишке.
В некоторых случаях лимфома затрагивает и нервную систему. При локализации болезни в мозговой оболочке могут появиться опасные расстройства неврологического характера, что может привести даже к параличу.
Помимо всех описанных областей поражения, лимфогранулематоз может локализоваться так же в:
- щитовидной железе,
- мягких тканях,
- яичниках,
- почках,
- вилочковой железе,
- молочных железах.
вилочковой железе,.
Как лечить лимфому
Основными методами лечения лимфомы являются оперативное вмешательство, лучевая и химическая терапии. В качестве вспомогательной терапии применяется народная медицина. Чем ниже степень злокачественности опухоли, тем выше шанс на выздоровление. Лимфома 4 стадия практически не поддается лечению и часто рецидивирует. Первая стадия лечится оперативным путем, поскольку область поражения небольшая. Химиотерапия при лимфоме проводится на всех стадиях. Некоторые виды опухолей не поддаются лечению при помощи облучения.

Кроме этих манипуляций, проводятся лабораторные и инструментальные исследования.





